Bildgebung bei Alzheimer
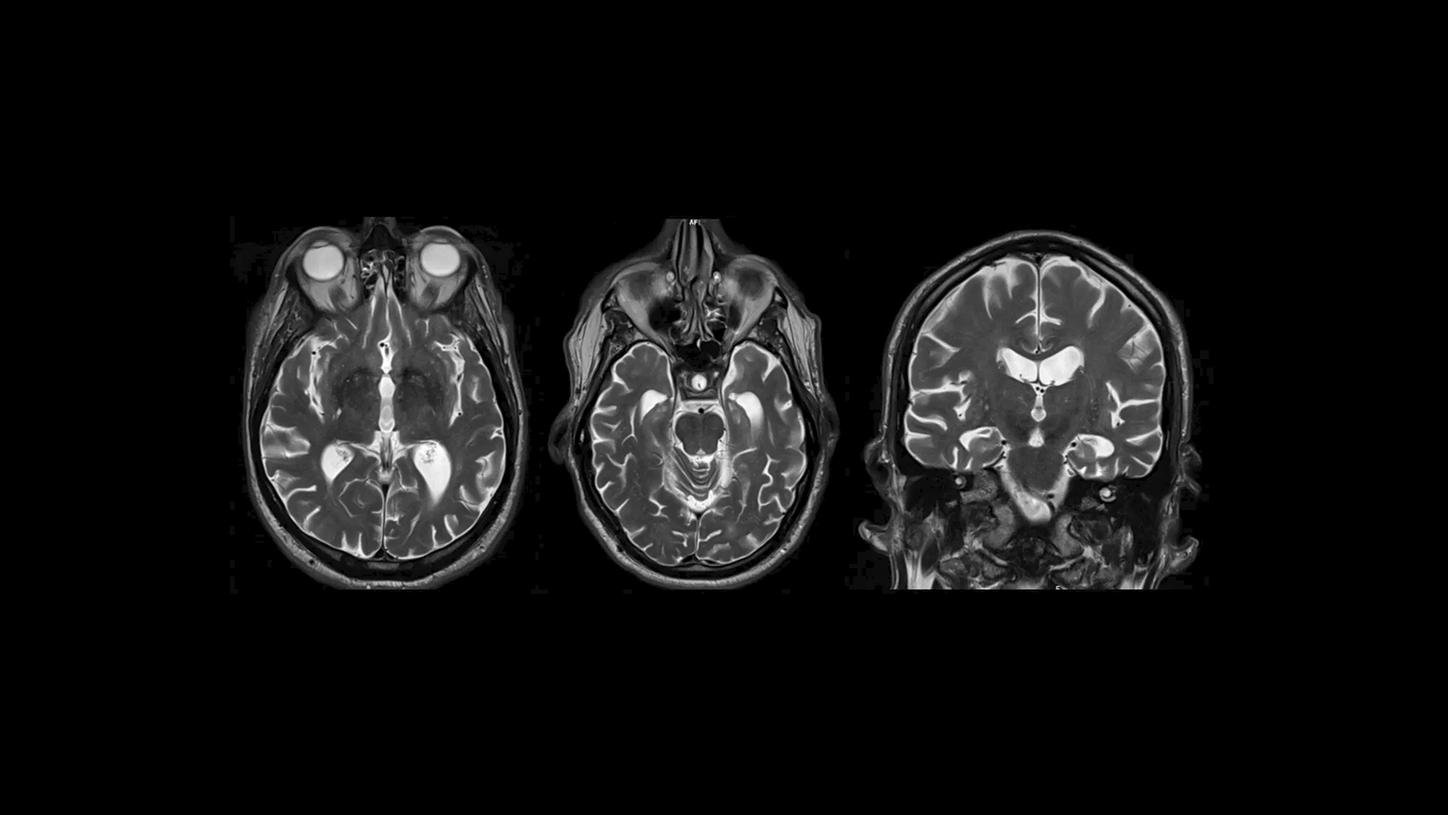
In der T2-MR-Bildgebung erscheinen Wasser und Liquor aufgrund ihrer hohen Signalintensität als helle Bereiche.
Für Alzheimer-Patienten kann ein rechtzeitiger Zugang zu MRT-Untersuchungen alles verändern. KI kann Scans um bis zu 50 Prozent beschleunigen, sodass mehr Patienten schneller untersucht werden können, was Behandlungsentscheidungen und Nachsorge erleichtert.
André Hartung, President Diagnostic Imaging, Siemens Healthineers.
PET/MR-Bild eines Patienten mit Alzheimer.2
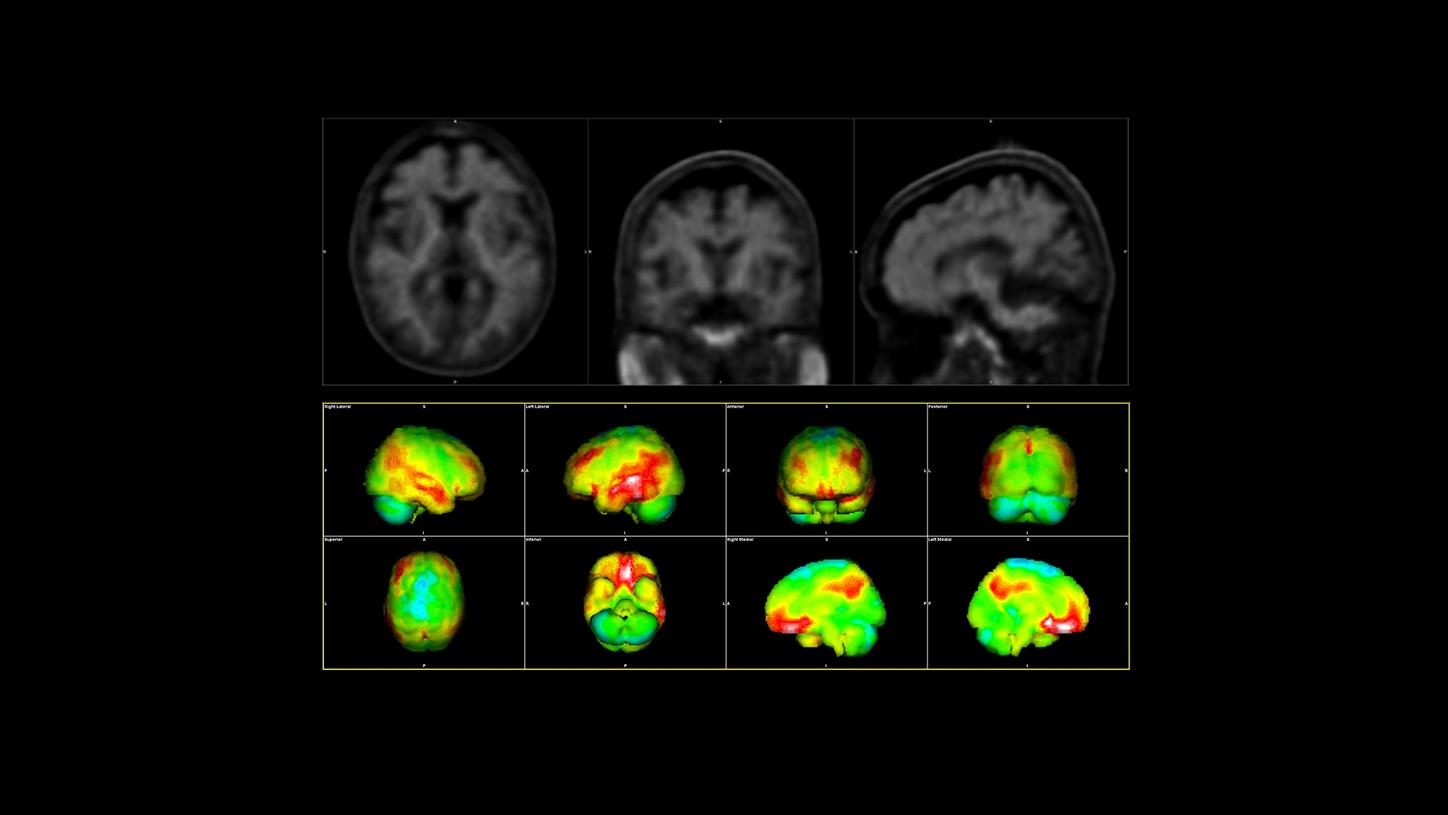
Ein typischer Amyloid-PET-Scan bei einem Alzheimer-Patienten: Die roten Bereiche sind die betroffenen Regionen im Gehirn.3
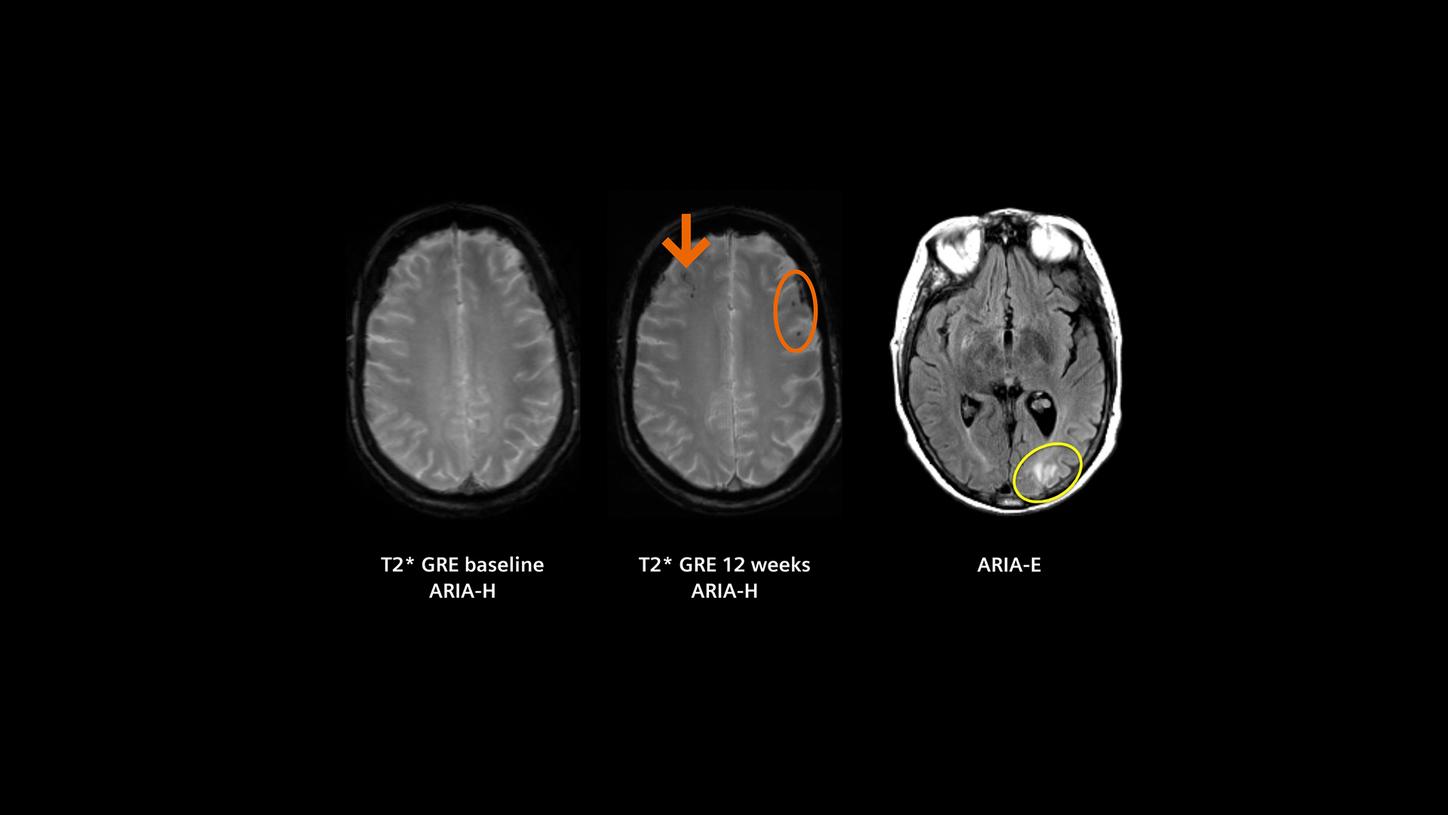
MR-Bilder Amyloid-bedingter Bildgebungsanomalien (ARIA-H und ARIA-E). Dies sind mögliche unerwünschte Nebenwirkungen der neuen krankheitsmodifizierenden Alzheimer-Therapien.4
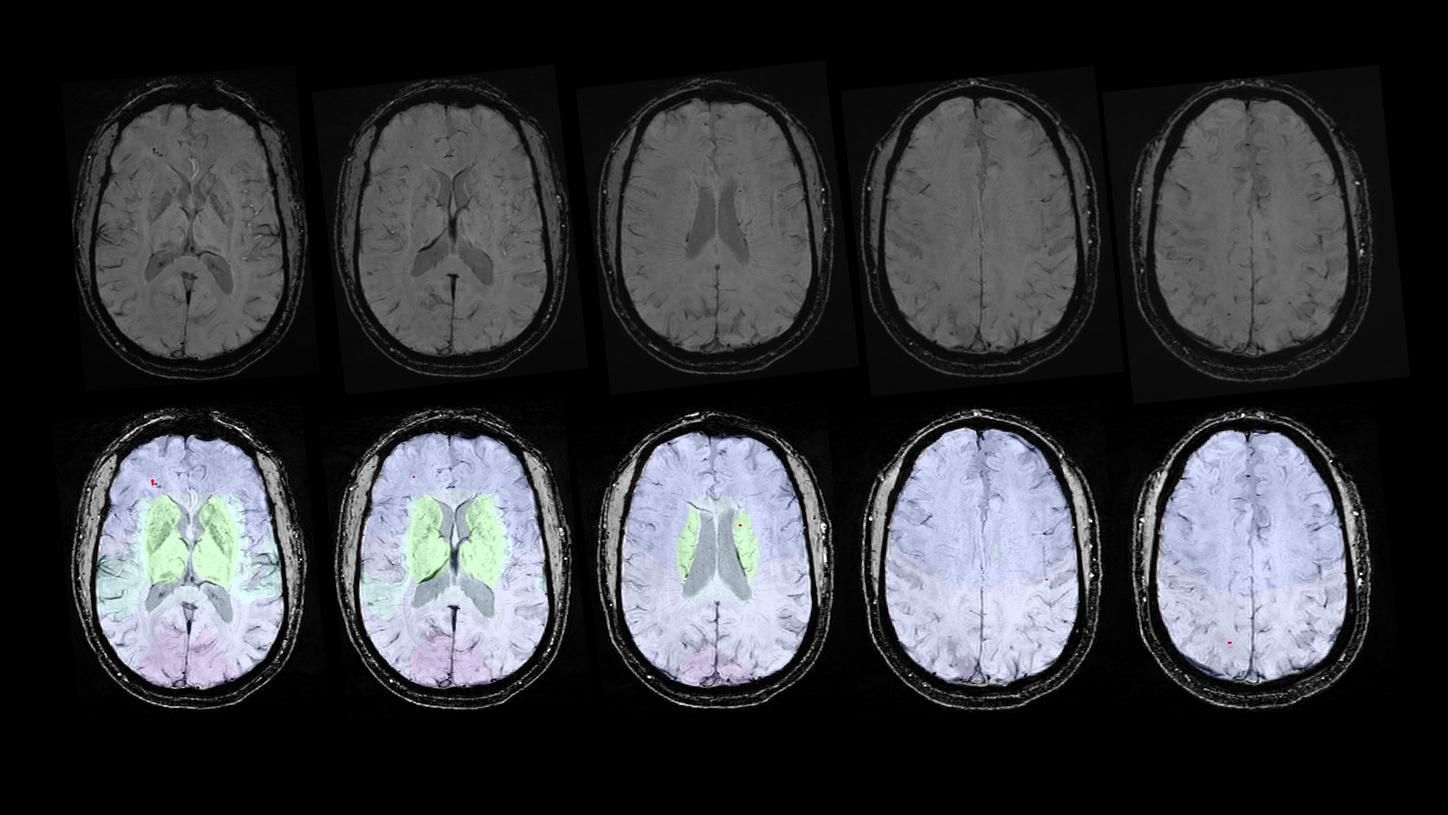
KI-gestützte Erkennung zerebraler Mikroblutungen (Prototyp).
1 Krankheitsmodifizierende Therapien (DMTs) für Alzheimer gehen mit gewissen Risiken einher. Informationen zu Nebenwirkungen, Kontraindikationen und Risiken finden Sie in der jeweiligen Therapiebeschreibung.
2 Erfasst mit dem Biograph mMR | Study-ID: 4aaaa0025 | Bild mit freundlicher Genehmigung des University Hospital Plzen, Tschechische Republik.
Bilder des Biograph mMR dienen der Veranschaulichung der typischen Fähigkeiten von PET/MR-Bildgebung und sind nicht spezifisch für den Biograph One. Der Biograph One steht noch unter dem Vorbehalt der 510(k)-Zulassung und ist in den Vereinigten Staaten noch nicht im Handel erhältlich. Die zukünftige Verfügbarkeit kann nicht garantiert werden.3 Daten mit freundlicher Genehmigung des Wentworth-Douglass Hospital, Dover, New Hampshire, USA.
4 Diese Anwendung ist nur für Forschungszwecke bestimmt und darf nicht zur Diagnose einzelner Patient*innen verwendet werden. Die genannte Anwendung ist möglicherweise nicht in allen Ländern verfügbar. Weitere Informationen über diese Forschungsanwendung und ihre Verfügbarkeit in Ihrem Land erhalten Sie von Ihrer Ansprechperson bei Siemens Healthineers.
Literaturverzeichnis
[1] Furtner J, Prayer D. Neuroimaging in dementia. Wien Med Wochenschr. 2021;171(11–12):274–81.
[2] Molinder A, Ziegelitz D, Maier SE, Eckerström C. Validity and reliability of the medial temporal lobe atrophy scale in a memory clinic population. BMC Neurol. 2021;21(1):289.
[3] Shi Q, Hou J, Peng X, Xu Z, Wang Y, Cao D. Magnetic resonance imaging analysis for Alzheimer's disease diagnosis using artificial intelligence: Methods, challenges, and opportunities. Ageing Res Rev. 2026;113:102943. Epub 2025 Nov 19.
[4] U.S. Food & Drug Administration. FDA to recommend additional, earlier MRI monitoring for patients with Alzheimer’s disease taking Leqembi (lecanemab). Current as of August 28, 2025. Accessed January 1, 2026. Available from: https://www.fda.gov/drugs/drug-safety-and-availability/fda-recommend-additional-earlier-mri-monitoring-patients-alzheimers-disease-taking-leqembi-lecanemab











